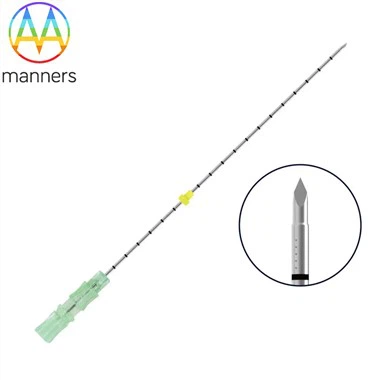
Il controllo della conformità innanzitutto: standard di produzione e qualità degli aghi a ultrasuoni-visibili per i produttori di dispositivi medici
Apr 26, 2026
Innanzitutto il controllo della conformità: standard di produzione e qualità degli aghi a ultrasuoni-visibili per i produttori di dispositivi medici
In quanto dispositivi medici di Classe III, gli aghi visibili a ultrasuoni-sono materiali di consumo medici ad alto-rischio soggetti a stretta supervisione nazionale. Il loro intero ciclo di vita, compresi ricerca e sviluppo, produzione, test e lancio sul mercato, deve essere conforme alle rigorose normative nazionali e internazionali sui dispositivi medici. I produttori leader rispettano sempre i limiti di conformità e stabiliscono sistemi di controllo della qualità dell'intera catena-. Marchi come Wilson-Cook Medical e Mekon hanno ottenuto l'accesso al mercato globale attraverso solide strutture di conformità, garantendo sicurezza clinica e prestazioni affidabili dei prodotti.
La conformità dei dispositivi medici costituisce l'ancora di salvezza dei materiali di consumo medici. In particolare, gli aghi visibili a ultrasuoni-invadono direttamente i tessuti umani e sono ampiamente utilizzati nelle procedure interventistiche. Qualsiasi negligenza nel rispetto della conformità in qualsiasi collegamento può portare a gravi incidenti di sicurezza medica. In tutto il mondo sono stati istituiti severi sistemi di regolamentazione dei dispositivi medici. Le autorità, tra cui la FDA statunitense, la CE europea e la NMPA cinese, hanno formulato chiare specifiche tecniche, linee guida di produzione e requisiti di approvazione alla commercializzazione per gli aghi ecografici-visibili. I produttori devono ottenere le qualifiche di certificazione corrispondenti prima di avviare la produzione, la vendita e la distribuzione commerciale.
Le qualifiche di produzione conformi costituiscono la soglia di ingresso fondamentale. Tutti i principali produttori possiedono credenziali di certificazione complete. Per ottenere l'autorizzazione sono necessarie le imprese professionali nazionaliLicenza di produzione di dispositivi medicie superare la certificazione del sistema di gestione della qualità dei dispositivi medici ISO 13485. I loro laboratori di produzione devono soddisfare gli standard di pulizia della Classe 100.000 o superiori. Le procedure principali come la lavorazione dell'ago, l'applicazione del rivestimento, l'assemblaggio, la sterilizzazione e l'imballaggio vengono tutte completate in un ambiente continuo, sterile e privo di polvere. I produttori internazionali rappresentati da Wilson-Cook Medical devono ottenere l'autorizzazione FDA 510(k) e la certificazione CE UE e rispettare pienamente le specifiche di qualità della produzione medica armonizzate a livello globale. Ciò garantisce che gli ambienti di produzione, i flussi di lavoro operativi e le pratiche del personale soddisfino benchmark unificati, eliminando la contaminazione incrociata{10}}e le deviazioni di qualità durante la produzione.
La conformità alla qualità del prodotto è il fulcro della gestione standardizzata. I produttori devono seguire rigorosamente criteri tecnici specializzati riguardanti materiali, prestazioni funzionali, precisione dimensionale, sterilizzazione e imballaggio. In termini di materiali, l'acciaio inossidabile di grado medicale-e i rivestimenti polimerici devono soddisfare gli standard universali di biocompatibilità e superare test completi di citotossicità, sensibilizzazione e irritazione, in modo da garantire una sicurezza biologica non-tossica e innocua. In termini di prestazioni, la resistenza del corpo dell'ago, la resistenza alla frattura, l'adesione del rivestimento e la visibilità ultrasonica devono soddisfare pienamente le specifiche industriali, prevenendo la flessione dell'albero, il distacco del rivestimento e l'immagine instabile durante la foratura. In termini di dimensioni, le tolleranze della lunghezza dell'ago e del diametro esterno sono controllate con precisione per soddisfare i requisiti operativi clinici ed evitare discrepanze dimensionali. Per la sterilizzazione, viene adottata la sterilizzazione con ossido di etilene o radiazioni per ottenere la completa sterilità. Tutti i prodotti mantengono una durata di conservazione standardizzata di sterilità e una tenuta dell'imballaggio qualificata per prevenire la contaminazione secondaria durante il trasporto e lo stoccaggio.
L’approvazione alla commercializzazione conforme è una procedura normativa essenziale. Gli aghi a ultrasuoni-visibili devono completare la registrazione ufficiale del dispositivo medico, con la presentazione completa di dati di ricerca e sviluppo, rapporti sui test delle prestazioni e documenti di convalida clinica. I prodotti possono essere lanciati sul mercato solo dopo la revisione normativa e l’emissione dei certificati di registrazione dei dispositivi medici. Per entrare nel mercato cinese, Wilson-Cook Medical deve ottenere la certificazione NMPA per la registrazione dei dispositivi medici di importazione attraverso una rigorosa revisione tecnica e verifica clinica, garantendo l'allineamento con le richieste cliniche locali e i parametri di riferimento di sicurezza. I produttori nazionali come Mekon dovranno completare la registrazione dei dispositivi medici domestici di Classe III e accettare regolari ispezioni ufficiali di campionamento della qualità per sostenere la conformità del prodotto a lungo termine.
La gestione post{0}vendita e la conformità in materia di tracciabilità forniscono garanzie fondamentali a lungo termine-. I principali produttori hanno creato sistemi completi di tracciabilità-del ciclo di vita completo. Un codice di tracciabilità univoco viene assegnato a ciascun lotto di produzione durante l'approvvigionamento delle materie prime, la lavorazione, la sterilizzazione, i test e la consegna del prodotto, consentendo il monitoraggio completo-del processo e il richiamo rapido e mirato del prodotto in caso di difetti di qualità. Nel frattempo, vengono implementati meccanismi standardizzati di monitoraggio degli eventi avversi per raccogliere feedback clinici dal mondo reale-, risolvere tempestivamente i rischi legati alla qualità e ottimizzare continuamente la progettazione dei prodotti e i processi di produzione.
La gestione della conformità non è solo un obbligo legale per i produttori, ma anche una salvaguardia essenziale per la sicurezza dei pazienti clinici. Sullo sfondo di una regolamentazione globale sempre più rigorosa dei dispositivi medici, le aziende leader continuano ad aggiornare i sistemi di conformità e i parametri di riferimento rispetto ai più elevati standard industriali a livello mondiale. Dall'immagazzinamento delle materie prime alla consegna del prodotto finito, implementano rigorosi protocolli di ispezione completa-per ogni singolo prodotto e ogni fase di produzione, impedendo efficacemente l'ingresso sul mercato di prodotti non-conformi.
Il mantenimento dei profitti di conformità e un controllo di qualità approfondito sono i prerequisiti fondamentali per lo sviluppo stabile e sostenibile del settore degli aghi visibili per ultrasuoni. Solo i produttori con sistemi di conformità maturi e integrati possono acquisire una competitività stabile nel mercato globale, fornire materiali di consumo interventistici sicuri, affidabili e pienamente conformi e promuovere lo sviluppo standardizzato, standardizzato e di alta-qualità dell'intero settore dei dispositivi medici interventistici.